Onze belangrijkste producten: Aminosiliconen, bloksiliconen, hydrofiele siliconen, al hun siliconenemulsies, bevochtigings- en wrijfvastheidsverbeteraar, waterafstotend (fluorvrij, koolstof 6, koolstof 8), demin-waschemicaliën (ABS, enzym, spandexbeschermer, mangaanverwijderaar). Voor meer informatie kunt u contact opnemen met: Mandy +86 19856618619 (Whatsapp)
Inleiding tot oppervlakteactieve stoffen
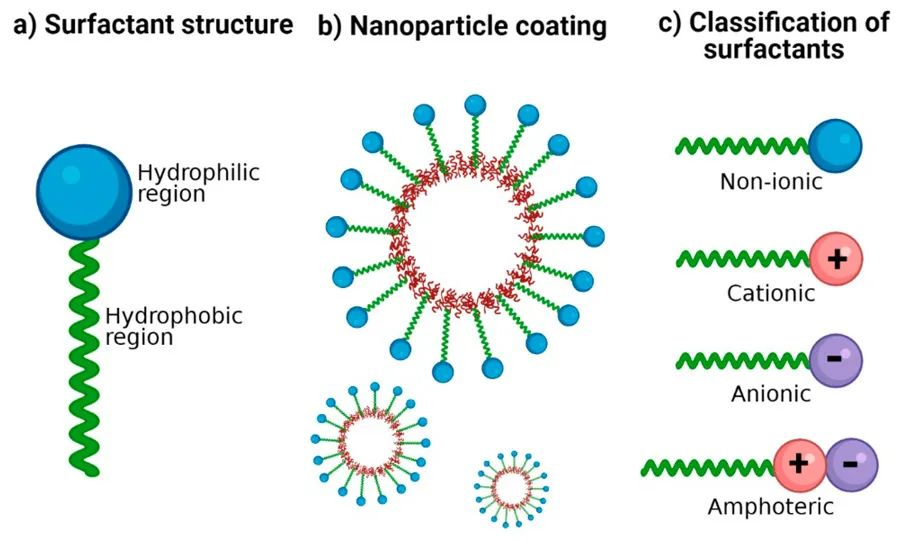
Oppervlakteactieve stoffen hebben een amfifiele moleculaire structuur: het ene uiteinde bevat een hydrofiele groep, de zogenaamde hydrofiele kop, terwijl het andere uiteinde een hydrofobe groep bevat, de zogenaamde hydrofobe staart. De hydrofiele kop zorgt ervoor dat oppervlakteactieve stoffen in hun monomeervorm in water oplossen.
De hydrofiele groep is vaak een polaire groep, die een carboxylgroep (-COOH), een sulfonzuurgroep (-SO3H), een aminogroep (-NH2), aminen en hun zouten, hydroxylgroepen (-OH), amidegroepen of etherverbindingen (-O-) kan zijn, als andere voorbeelden van polaire hydrofiele groepen.
De hydrofobe groep is doorgaans een niet-polaire koolwaterstofketen, zoals hydrofobe alkylketens (R- voor alkyl) of aromatische groepen (Ar- voor aryl).
Oppervlakteactieve stoffen kunnen worden onderverdeeld in ionische oppervlakteactieve stoffen (waaronder kationische en anionische oppervlakteactieve stoffen), niet-ionische oppervlakteactieve stoffen, amfotere oppervlakteactieve stoffen, gemengde oppervlakteactieve stoffen en andere. Wanneer de concentratie van een oppervlakteactieve stof in oplossingen een bepaalde waarde bereikt, vormen de moleculen van de oppervlakteactieve stof verschillende geordende aggregaten, micellen genaamd. Het proces van micellisatie, of micelvorming, is een cruciale fundamentele eigenschap van oplossingen van oppervlakteactieve stoffen, aangezien veel belangrijke grensvlakverschijnselen samenhangen met de vorming van micellen.
De concentratie waarbij oppervlakteactieve stoffen micellen vormen in oplossing wordt de kritische micelconcentratie (CMC) genoemd. Micellen zijn geen vaste, bolvormige structuren; ze vertonen juist extreme onregelmatigheden en dynamische vormveranderingen. Onder bepaalde omstandigheden kunnen oppervlakteactieve stoffen ook omgekeerde miceltoestanden vertonen.
Factoren die CMC beïnvloeden:
- Structuur van de oppervlakteactieve stof
- Type en aanwezigheid van additieven
- Temperatuur
Interacties tussen oppervlakteactieve stoffen en eiwitten
Eiwitten bevatten apolaire, polaire en geladen groepen, en veel amfifiele moleculen kunnen op verschillende manieren met eiwitten interacteren. Afhankelijk van de omstandigheden kunnen oppervlakteactieve stoffen moleculair georganiseerde aggregaten vormen met verschillende structuren, zoals micellen of omgekeerde micellen, die op verschillende manieren met eiwitten interacteren.
De interacties tussen eiwitten en oppervlakteactieve stoffen (Protein-Surfactant, PS) bestaan voornamelijk uit elektrostatische en hydrofobe interacties. Ionische oppervlakteactieve stoffen interageren voornamelijk met eiwitten via de elektrostatische krachten van de polaire groep en de hydrofobe interacties van de alifatische koolstofketen, waarbij ze zich binden aan de polaire en hydrofobe delen van het eiwit en zo PS-complexen vormen.
Niet-ionogene oppervlakteactieve stoffen interageren voornamelijk met eiwitten via hydrofobe krachten, waarbij de hydrofobe ketens interacteren met de hydrofobe delen van de eiwitten. Deze interactie kan zowel de structuur als de functie van de oppervlakteactieve stof en het eiwit beïnvloeden. Daarom bepalen het type en de concentratie van de oppervlakteactieve stof, samen met de omgevingscontext, of oppervlakteactieve stoffen eiwitten stabiliseren of destabiliseren, en of ze aggregatie of dispersie bevorderen.
HLB-waarde van oppervlakteactieve stoffen
Om zijn unieke grensvlakactiviteit te kunnen uitoefenen, moet een oppervlakteactieve stof een evenwicht vinden tussen de hydrofobe en hydrofiele componenten. De HLB (Hydrofiel-Lipofielbalans) is een maatstaf voor de hydrofiele-lipofiele balans van oppervlakteactieve stoffen en dient als indicator voor de hydrofiele en hydrofobe eigenschappen van de oppervlakteactieve stoffen.
De HLB-waarde is een relatieve waarde (variërend van 0 tot 40). Paraffine heeft bijvoorbeeld een HLB-waarde van 0 (geen hydrofiele component), polyethyleenglycol heeft een HLB-waarde van 20 en het zeer hydrofiele SDS (natriumdodecylsulfaat) heeft een HLB-waarde van 40. De HLB-waarde kan dienen als referentie bij de selectie van oppervlakteactieve stoffen. Een hogere HLB-waarde duidt op een betere hydrofiliteit, terwijl een lagere HLB-waarde een slechtere hydrofiliteit suggereert.
Plaatsingstijd: 10-09-2024

